01 · 反应热与焓变 整理中
热化学方程式
热化学方程式
(1)概念:表明反应所释放或吸收的热量的化学方程式。
(2)意义:表明了化学反应中的物质变化和能量变化。
在
书写热化学方程式的注意事项
(1)
(2)需注明反应时的温度和压强。如不注明,即专指
(3)不用写加热、加压、催化剂、沉淀、气体等反应条件或符号。但必须注明各物质的状态:固体—
(4)热化学方程式中化学计量数可为整数或分数,其表示参加反应的各物质的物质的量,因此
(5)若反应逆向进行,则
(6)若反应为可逆反应,
燃烧热
1.定义:
2.熟记常见元素完全燃烧生成的指定产物
| 元素 | C | H | S | N |
|---|---|---|---|---|
| 指定产物及状态 |
3.
4.燃烧热的热化学方程式 书写燃烧热的热化学方程式时,以燃烧
燃烧热的测量
测定原理:将待测物质放在一个充满氧气的密封金属容器(称为氧弹)内,再将此容器置于盛有一定量水的量热计内筒中,通过点火装置使氧弹中物质燃烧,反应放出的热量会使氧弹外面的水温升高。用温度计测量水温的变化,即可计算出此反应放出的热量。
中和反应反应热的测定实验
请按照下列步骤,用简易量热计 (如图) 测量盐酸与 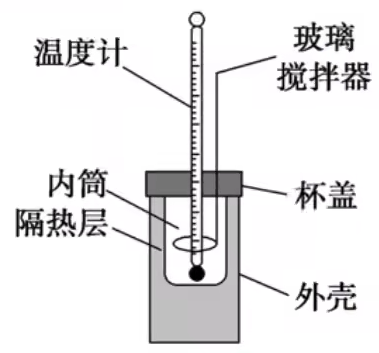
1.反应物温度的测量
(1) 用量筒量取
(2) 用另一个量筒量取
2.反应后体系温度的测量打开杯盖,将量筒中的
3.重复上述步骤 1 至步骤 2 两次.
【数据处理】
(1) 取盐酸温度和
| 实验次数 | 反应物的温度 /℃ | 反应物的温度 /℃ | 反应前体系的温度 | 反应后体系的温度 | 温度差 |
| 盐酸 | $\ce{NaOH}$ 溶液 | $t_1$/℃ | $t_2$/℃ | $(t_2-t_1)$/℃ | |
| 1 | |||||
| 2 | |||||
| 3 |
(2) 取三次测量所得温度差的平均值作为计算依据
(3) 根据温度差和比热容等计算反应热
(4) 实验数据处理
数据处理计算
1.反应原理:
2.为了计算简便,可以近似地认为实验所用酸、碱稀溶液的密度、比热容与水的相同,并忽略量热计的比热容,
则:①
②反应后生成的溶液的比热容
为了提高测定的准确度,应该采取哪些措施?
1.隔热层、杯盖等的使用是为了减少热量散失,降低实验误差.
2.要使用同一支温度计,避免仪器误差.注意测定一种溶液后必须用水冲洗干净并用滤纸擦干.
3.使用不同的量筒分别量取酸碱溶液
4.正确读取体积和温度,多次试验求平均值时,若有某一组的实验数据有明显偏差,应直接舍去.
5.操作时动作要快,尽量减少热量的散失
6.为了保证盐酸完全被中和,采用稍过量的
吸放热反应的判断
依据化学键能量变化:对比反应物断键吸收的能量与生成物成键释放能量的多少(断键吸热 > 成键放热为吸热反应,反之则为放热反应)。
依据物质总能量:反应物总能量 > 生成物总能量为放热反应,反之则为吸热反应。
提示:放热反应与放热过程不同,放热反应有新物质生成(如燃烧),放热过程无新物质生成(如水蒸气液化)。
典型的吸热反应与放热反应
典型吸热反应:绝大多数分解反应、铵盐与碱的反应、
典型放热反应:燃烧与中和反应、绝大多数化合与氧化还原反应、铝热反应、金属与酸 / 水的置换反应、氯酸钾分解、双氧水分解。